
研究員のつむぎです。
今回は、コアシェルエレクトロスピニングナノファイバーに基づく限局性がん光線力学療法アプローチについて調べました!
研究員:つむぎ
MECCのナノファイバー部門に所属して2年目の研究員。
趣味:科学雑誌や最新の研究論文を読むこと、空手
特技:中国語
【背景と目的】
子宮頸がんは女性の間で4番目に多いがんです。治療法として手術や放射線治療、化学療法が挙げられますが、副作用が多く有効性も制限されてしまいます。そこで、副作用を最小限に抑え再発を防ぐために、光線力学療法(PDT)などの代替治療が検討されています。
PDTは、光増感剤と呼ばれる光活性分子(PS)を投与してがん細胞に吸収させ、標的部位に特定の波長を照射することでPSが活性化されて、発生した一重項酸素により様々な生体分子が酸化され標的組織が不可逆的に破壊されるという原理の治療法です。
PSには、ポルフィリン(Por)とその誘導体がよく利用されています。Porは一重項酸素量子収率の高さや最小限の暗所毒性を有し、体内から速やかに除去されるなどの利点がある一方で、全身投与では安定した効果を発揮するために必要な投与量が多く光感受性の長期化につながることや、腫瘍局所を標的とするまでに化合物が消失する可能性があるなど、いくつかの欠点も挙げられます。
筆者らはこれらの欠点を解決するためにPSを局所薬物送達システム(DDS)に組み込もうと考えました。腫瘍部位またはその付近に局所DDSを埋め込むことで、標的部位にPSを直接送達でき、治療効果の上昇、周囲の健康な細胞に対する副作用の低減、持続的なPS放出の可能性、標的到達前のPS分解からの保護、PSの凝集防止、薬剤の投与回数を一度にできるといった利点が挙げられます。
エレクトロスピニング技術は簡便にナノファイバーを作製できて、様々な要件に適応できる汎用性の高い技術であり、局所的なDDSとして機能するナノファイバーの開発においても注目を集めています。エレクトロスピニングナノファイバーは対比表面積が高くがん治療におけるDDSのベースとして際立っており、効率的な薬物封入、材料と治療薬の幅広い選択肢などの点から、標的特異的な薬物送達、複数薬物の同時封入、薬物プロファイルの制御を可能にします。また、細胞外マトリックスに似た構造を持ち、薄く小型で柔軟性を持つため小さな隙間にも入り込むことが可能です。子宮頸がん治療では、膣管からアクセス可能で、DDSを腫瘍細胞もしくは周辺に移植し、照射ができるため非常に有望です。また、光線治療ナノファイバーは、診断と治療を同時に行えるようになります。
コアシェル型ナノファイバーは、同軸エレクトロスピニング法を利用して2種類の異なるポリマー溶液を同時に使用することで作製できます。この2種類のポリマーを合成高分子の機械的強度と天然高分子の生物学的活性の組み合わせにすることで、DDS開発の有効な戦略となります。コアは生理活性分子の単体として、シェルはその分解や早期放出を防ぐ保護層として機能します。 局所的なDDSとしてのナノファイバーと、がん治療としてのPDT利点は十分に確立されていますが、両者を組み合わせた治療法はまだ十分に検討されていません。そこで筆者たちは、PDTの局所的なDDSとして作用するPS剤であるPorを担持したコアシェルエレクトロスピニングナノファイバーを開発することを目的とし研究を行いました。

がん治療で注目されている方法の組み合わせですね。
〈材料〉
ポリビニルアルコール(PVA)、ゼラチン(Gel)、合成Por
〈方法〉
Porを合成して一重項酸素と光線力学的作用を評価したのち、エレクトロスピニング技術を利用して、コアシェルエレクトロスピニングナノファイバーにPorを組み込みました。この際、コア層にPVA、シェル層にはGelを使用しています。そして、エレクトロスピニングにより作製されたナノファイバーを特性評価し、腫瘍細胞株及び非腫瘍細胞株に対する暗所条件下および放射線照射下での比較、薬物放出プロファイルを評価しました。
〈結果〉
・腫瘍細胞株及び非腫瘍細胞株でのPorの一重項酸素発生と細胞毒性
すでに発表されている実験手順から5,10,15,20-テトラキス(4-カルボキシメチルチオ-2,3,5,6-テトラフルオロフェニル)ポルフィリン(TPPF16[S-CH2-COOH]4)の合成を行いました。
TPPF16[S-CH2-COOH]4の一重項酸素発生能は、テトラフェニルポルフィリン(TPP)の結果と同程度の生成能であることが確認できたため、以下の実験に利用していきます。
次に、腫瘍細胞・非腫瘍細胞に対する細胞毒性を評価しました。細胞増殖を50%阻害するために必要なPor濃度(GI50値)を見ると、暗所条件下と比較すると光照射下では非常に低い値を示しました。これにより、腫瘍細胞の増殖を阻害するためには非常に低濃度のPorが必要であり、PSが光照射下で高い細胞毒性を示しがん細胞に対する光線力学的効率が実証されました。また、非腫瘍細胞でのGI50値から暗所条件下と光照射時どちらも高濃度のPorが必要であることが示され、Porが非腫瘍細胞よりも腫瘍細胞に対して細胞毒性が高いことを裏付けています。
さらに、Porは腫瘍細胞に対して光照射条件下では暗所条件の11倍の光毒性を示し、非腫瘍細胞ではわずか2倍であったことから、Porの光毒性は非腫瘍細胞では軽減されることを示しました。
・PVA-ゼラチンコアシェルナノファイバーへのPorの組み込み PVA-ゼラチンコアシェルナノファイバーは同軸エレクトロスピニング法を利用して作製した。同軸アクセサリーは画像のものを作製した。

(Sofia M. Costa, Leandro M. O. Lourenço, Ricardo C. Calhelhacd, et al. : Localized cancer photodynamic therapy approach based on core–shell electrospun nanofibers, Materials Advances , Issue 16, 6489-6500,21th August 2024. より引用)

使用されたスピナレットは、弊社で販売している芯鞘スピナレットです!
作製したナノファイバーはFESEM、TEM、TGA、ATR-FTIRにより特徴づけられ、PVAとゼラチンの両方のポリマーが存在していて、表面が滑らかで欠陥のないナノファイバーであることが確認できました。
Porをナノファイバーに組み込む際にGI50値を考慮し、4種のPor濃度のナノファイバーを作製し、評価・分析を行いました。
PVAにPorを添加するとPor濃度に応じて溶液の粘度・導電率が増加しました。これは、Por組み込みにより電荷密度が増加し、導電率値が上昇し放出されるジェットの伸び力が強くなったことで、繊維径の減収が促進されていると考えられます。

繊維径は平均125nmとかなり細くなっていたようです。
ナノファイバー中のPorの存在確認をGSDRにて行いました。PSの特徴的な吸収帯が見られ、得られたスペクトルはPorのみのスペクトルと非常に類似しており、ナノファイバーへのPorの存在が確認され、Por濃度を上げるとバンドの強度が増加しました。
繊維内のPor分布はCLSMにより評価されました。ナノファイバーを405 nmで励起し、放出された蛍光を500-699 nmで検出しました。PVA-ゼラチンナノファイバーでは、405nmで励起しても蛍光は検出されませんでしたが、Por を担持した PVA-ゼラチン+Porナノファイバーでは赤色蛍光が検出されました。この蛍光がファイバーに沿って連続していることから、Porは凝集することなく全体に分布していることがわかります。
また、エレクトロスピニングナノファイバーは、高い担持能と高いカプセル化効率を特徴としており、薬物送達への非常に魅力的なプラットフォームとなっています。PVA-ゼラチン+Porナノファイバーの担持能とカプセル化効率を測定した結果、どちらも高い値を示し、DDSに適していることが実証されました。
GSDR、CLSMの結果から、PSをエレクトロスピニングナノファイバーに組み込むことに成功したことが確認できます。さらに、繊維内のPorカプセル化はその特性に影響がなく、固有の蛍光特性によるリアルタイムの治療モニタリングパラメーターや治療反応評価を可能にし、その後の治療プログラムの計画や調整が可能になります。
・コアシェルナノファイバーからのPor放出プロファイル
作製したナノファイバーを膣内環境に近づけた溶液に浸し撹拌した際のPorの放出をUV-Vis分光法によって観察しました。
PVA-ゼラチンナノファイバーとPVA-ゼラチン+Porナノファイバーを用いて得られた吸収スペクトルと薬物放出プロファイルをグラフにして表しました。
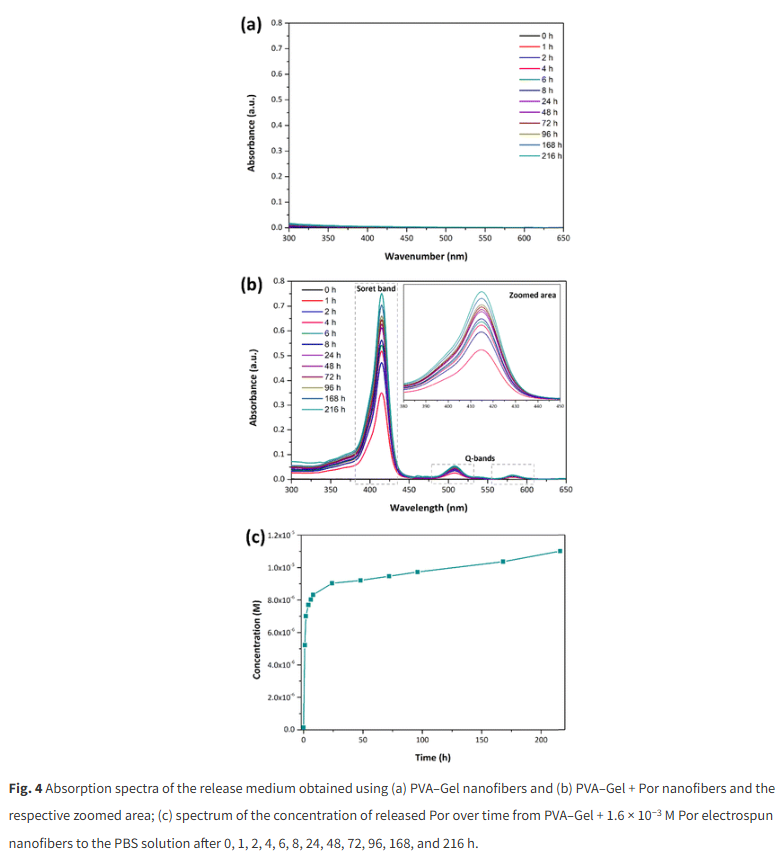
(Sofia M. Costa, Leandro M. O. Lourenço, Ricardo C. Calhelhacd, et al. : Localized cancer photodynamic therapy approach based on core–shell electrospun nanofibers, Materials Advances , Issue 16, 6489-6500,21th August 2024. より引用)
PVA-ゼラチン+Porナノファイバーのスペクトルでのみ典型的な吸収バンドの出現がみられ、時間の経過とともにPorが放出されることを示しました。
ナノファイバーからの薬物放出プロファイルには薬物の物理学的特性やポリマーマトリックスの構造特性、放出条件などいくつかの起因が寄与します。コアシェルナノファイバーでは、カプセル化された分子がコア層とシェル層の両方のマトリックスを通過する必要があり、より持続的な薬物放出を可能にします。
さらにPorの放出を評価するためにStoreバンドのズームを行ったところ、1時間~8時間でバンドの存在が観察されました。これはエレクトロスピニング中にPVAが漏れ繊維表面の一部に露出している可能性があり、Porの迅速な放出が促進されます。その後Porは時間をかけて徐々に放出されました。この結果は、ナノファイバーのコアから溶液中への分子の拡散を可能にしたコアシェル構造の劣化に関連する可能性があります。
また、時間の経過に伴うPor濃度のプロットも行ったところ、最初の数時間は高速薬物放出ファイルを観察し、その後持続的かつ徐々に放出されることが確認できました。この結果からシェル層の存在がPorの拡散を遅らせている可能性があります。
これらの結果から、最初の早い放出以降は持続的にPorが放出されることを示しており、PVA-ゼラチン+Porナノファイバーが子宮頸がん治療に対して持続的で連続的なDDS機能を有することが確認できました。
・腫瘍細胞株および非腫瘍細胞株におけるエレクトロスピニングナノファイバーの細胞毒性試験
Porがナノファイバー膜に取り込まれた状態でPSとして作用する能力を評価するために、PVA-ゼラチンナノファイバーおよびPVA-ゼラチン+Porナノファイバーの細胞毒性試験を行いました。ナノファイバーで細胞をインキュベートしメンブレンを除去したのち細胞にLEDランプを照射しました。結果は以下の表になります。
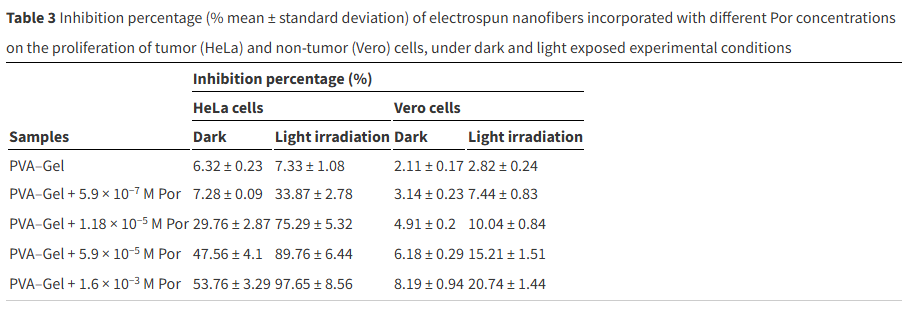
(Sofia M. Costa, Leandro M. O. Lourenço, Ricardo C. Calhelhacd, et al. : Localized cancer photodynamic therapy approach based on core–shell electrospun nanofibers, Materials Advances , Issue 16, 6489-6500,21th August 2024. より引用)
PVA-ゼラチンナノファイバーは腫瘍細胞に対する暗所条件下及び光照射下ともに低い阻害率を示し、最小限の細胞毒性を示しました。両条件下での数値も類似しており、照射下での特性が示されていないことが確認できます。
PVA-ゼラチン+Porナノファイバーでは、腫瘍細胞に対して暗所条件下および光照射下での阻害を促進し、この阻害割合はPor濃度に比例していました。とくに、暗所条件下よりも光照射下での阻害率が非常に高く、Porがナノファイバーに取り込まれた後でも光毒性が残っていることを示しています。
また、最小限のPor添加量でも光線力学効果を達成できているため、暗所毒性や皮膚光過敏症を回避できます。
今回の実験では細胞に24時間ナノファイバーを接触させたのち除去しているため、観察された光毒性効果がその期間後に放出された分子によるものになります。薬物放出試験によりナノファイバーからのPorの放出は少なくとも216時間まで確認できており、ナノファイバーが長期間の放出に応用でき、薬物の反復投与を避けられることを示唆しています。
PVA-ゼラチンナノファイバーは非腫瘍細胞に対して非常に低い毒性を示し、光に対する特異性を示さず細胞増殖阻害も腫瘍細胞で観察された値より一貫して低く、暗所条件下と光照射下で得られた値の差もかなり低かったことから、腫瘍細胞株に選択的な光細胞毒性作用があることを示唆しています。
これらの結果から、Por分子の光線力学的効果はナノファイバーへの組み込みによる影響を受けず、光照射下で腫瘍細胞を破壊できる光活性分子を運ぶ基質となる可能性が示されました。これらの繊維状プラットフォームは腫瘍細胞株において選択的な光細胞毒性を有し、非腫瘍細胞に対する安全性を維持しながら腫瘍細胞を治療するPDTアプローチへの適合性と可能性を強調しています。
〈まとめ〉
同軸エレクトロスピニング技術を利用することにより、光応答性コアシェルナノファイバーを開発しました。このナノファイバーは生分解性ポリマーであるPVAとゼラチンを用いて作製し、コアには異なる濃度のPorが組み込まれています。
合成されたPorは一重項酸素を生成し、腫瘍細胞に対して光照射下ではるかに高い細胞毒性を示したことから、PDT用のPSとして機能する有望な候補であることが示されました。Porはナノファイバーの形態に影響を与えることなく組み込むことができ、ナノファイバー全体に分布していました。
これらの繊維状ナノプラットフォームはPorの高い担持能と高いカプセル化効率を示し、ナノファイバーからPor放出は9日間連続的に放出されました。初期段階は放出が早く、その後ゆっくりと持続的な放出が続いていました。これはナノファイバーのコアシェル構造によるものだと考えられます。
PVA-ゼラチン+Porナノファイバーは光線力学的効果を示しました。腫瘍細胞の増殖を抑制する割合が暗所条件下よりも光照射下で高かったことから、PVA-ゼラチン+Porナノファイバーが放射線に曝されたとき、腫瘍細胞の増殖を抑制する能力があることが確認でき、さらに腫瘍細胞株では、非腫瘍細胞株と比較して選択的な光細胞毒性作用がみられました。 本研究ではPSを組み込んだナノファイバーが、がんPDT特に子宮頸がんに対する局所的なDDSとして機能し、Porの連続放出を可能にする大きな可能性を示しています。

前回もエレクトロスピニングナノファイバーによるDDSの文献を紹介させていただきましたが、用途や材料の組み合わせ・作製方法によって異なる治療法に応用でき、ナノファイバーの汎用性を改めて実感しました!
副作用の少なく効果的ながん治療のためにコアシェルナノファイバーによるDDSはとても効果的ですね。
がんに罹患される方が日本でも年々増えているため、この研究がさらに進むことで罹患された方の治療が、副作用がなく効果的なものになりそうですね☻今後の進展に期待大です!!!
弊社では、様々なナノファイバーサンプルを作製しております。
試したい材料や紡糸に関する質問があれば、お気軽にご連絡ください。
【参考文献】
〈Localized cancer photodynamic therapy approach based on core–shell electrospun nanofibers〉
コアシェルエレクトロスピニングナノファイバーに基づく限局性がん光線力学療法アプローチ
Sofia M. Costa, Leandro M. O. Lourenço, Ricardo C. Calhelhacd, Isabel Calejo, Cristina C. Barrias, Raul Fangueiro and Diana P. Ferreira
(Centre for Textile Science and Technology (2C2T), University of Minho, 4800-058 Guimarães, Portugal.) (https://pubs.rsc.org/en/content/articlelanding/2024/ma/d4ma00647j)
